La maladie de Parkinson est un trouble courant qui survient en raison d’une imperfection qui modifie le fonctionnement normal du système nerveux central. La maladie de Parkinson est le résultat de la mort des cellules contenant de la dopamine de la région du mésencéphale identifiées comme substantia nigra. La raison de la mort de ces cellules n’est toujours pas identifiée. Les symptômes immédiats de la maladie sont des problèmes liés au mouvement comme des tremblements, une rigidité, une lenteur des mouvements et des difficultés à marcher et à marcher.
Au fur et à mesure que la maladie progresse, le patient souffre de troubles cognitifs ainsi que de problèmes de comportement. La démence est la caractéristique la plus protubérante dans les phases avancées de la maladie. Les autres symptômes secondaires sont le sommeil, les problèmes émotionnels et sensoriels. Cette maladie se rencontre généralement chez les personnes âgées qui ont franchi la cinquantaine. Lorsque les principaux symptômes moteurs sont pris en compte, la maladie est appelée parkinsonisme ou syndrome parkinsonien. Ce trouble est parfois également classé dans la catégorie idiopathique, bien que dans certains cas, l’origine génétique joue également un rôle clé. Des études ont clairement indiqué que le danger de la maladie de Parkinson augmente si les individus sont exposés à certains pesticides, bien que le risque diminue chez les fumeurs de tabac.
Du point de vue pathologique, la maladie de Parkinson apparaît en raison de l’accrétion d’une protéine connue sous le nom d’alpha-synucléine sous forme d’inclusions. Ces inclusions sont désignées par le terme corps de Lewy qui s’accumule dans les neurones. La formation et la fonction inadéquates de la dopamine dans certaines zones spécialisées du mésencéphale sont également considérées comme responsables de la maladie de Parkinson.
La lévodopa et les agonistes de la dopamine se sont avérés efficaces dans le traitement des premiers symptômes de la maladie. Au fur et à mesure que la maladie progresse, les neurones dopaminergiques finissent par se perdre des régions du mésencéphale et un stade arrive où les médicaments deviennent inutiles pour traiter les premiers symptômes. Lorsque ce stade est atteint, un autre obstacle appelé dyskinésie apparaît, associé à des mouvements de contorsion involontaires.
L’alimentation et certains types de rééducation peuvent cependant aider à réduire certains symptômes. Lorsque les médicaments deviennent inefficaces, la chirurgie et la stimulation cérébrale profonde sont la solution ultime car elles peuvent réduire les symptômes moteurs. Des études menées sur des modèles animaux ont montré que les greffes de cellules souches, la thérapie génique et les agents neuroprotecteurs peuvent aider à réduire les symptômes désastreux de la MP.
Des médicaments pour les troubles du sommeil et les problèmes émotionnels sont également accessibles. La maladie porte le nom du médecin anglais James Parkinson qui a donné le premier compte rendu détaillé de la maladie dans An Essay of the Shaking Palsy en 1817. La tulipe rouge est l’icône de cette maladie et la journée mondiale de la maladie de Parkinson est célébrée à la mémoire du Dr Parkinson le 11 avril. Michael J. Fox et Muhammad Ali sont des personnalités renommées qui ont également souffert de cette maladie et ont contribué à faire prendre conscience des conséquences et du traitement de la maladie de Parkinson.
Classification
Le terme parkinsonisme est appliqué à un syndrome moteur dont les principaux symptômes sont des tremblements au repos, une raideur, un ralentissement des mouvements et une instabilité posturale. Le syndrome parkinsonien peut être classé en quatre catégories selon l’origine des symptômes.
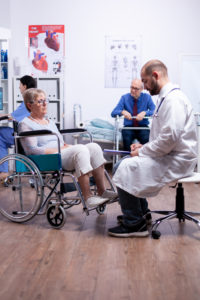 Ces sous-types sont primitifs ou idiopathiques, secondaires ou acquis, héréditaires parkinsoniens et syndromes Parkinson plus. La maladie de Parkinson est le type de parkinsonisme le plus courant, également connu sous le nom de parkinsonisme primaire, mais la cause applicable de cette maladie est encore mystérieuse. Au cours des dernières années, des études ont montré que les gènes jouent un rôle primordial dans ce trouble. La maladie de Parkinson est généralement classée comme un trouble du mouvement, mais elle est également responsable de nombreux problèmes non moteurs tels que des problèmes sensoriels, des troubles cognitifs et des troubles du sommeil.
Ces sous-types sont primitifs ou idiopathiques, secondaires ou acquis, héréditaires parkinsoniens et syndromes Parkinson plus. La maladie de Parkinson est le type de parkinsonisme le plus courant, également connu sous le nom de parkinsonisme primaire, mais la cause applicable de cette maladie est encore mystérieuse. Au cours des dernières années, des études ont montré que les gènes jouent un rôle primordial dans ce trouble. La maladie de Parkinson est généralement classée comme un trouble du mouvement, mais elle est également responsable de nombreux problèmes non moteurs tels que des problèmes sensoriels, des troubles cognitifs et des troubles du sommeil.
Les symptômes du parkinsonisme primaire comprennent une atrophie multisystémique, une paralysie supranucléaire progressive, une dégénérescence corticobasale et une démence à corps de Lewy. Du point de vue physiopathologique, le parkinsonisme est considéré comme une synucléinopathie car il existe une accumulation anormale de protéine alpha-synucléine sous forme de corps de Lewy dans le cerveau. Cette condition peut être assimilée à la maladie d’Alzheimer car il y a une accumulation de protéine tau sous la forme d’enchevêtrements neurofibrillaires inexplicables. Des études ont indiqué qu’il existe une intersection clinique et pathologique entre les tauopathies et les synucléinopathies. Les enchevêtrements neurofibrillaires ont été séparés du cerveau des patients atteints de MP. La démence à corps de Lewy (DLB) a des ressemblances avec la MP. L’association méticuleuse entre PD et DLB n’est toujours pas claire.
Symptômes
La maladie de Parkinson provoque des difficultés liées au mouvement entraînant des problèmes moteurs. Outre les problèmes moteurs, les problèmes non moteurs comme le dysfonctionnement autonome, les problèmes neuropsychiatriques suivis de troubles sensoriels et de sommeil montrent également leur présence dans les phases avancées de la maladie. Quatre problèmes moteurs sont considérés comme graves dans ce trouble et ce sont les tremblements, la rigidité, la lenteur des mouvements et l’instabilité posturale.
Le tremblement est le symptôme très fréquemment observé de la maladie de Parkinson. Dans environ 30% des cas, les tremblements ne surviennent pas comme le premier symptôme du trouble mais se développent plus tard à mesure que la maladie progresse. Parmi les tremblements, la fréquence du tremblement de repos est élevée et il s’intensifie lorsque le membre est au repos mais s’estompe lorsqu’une action volontaire est exécutée ou que le patient dort. Le tremblement de repos est connu pour perturber d’abord la partie distale du membre. Au début, seule la main ou la jambe est englobée, mais à mesure que la maladie progresse, ce tremblement devient bilatéral. La fréquence du tremblement varie entre 4 et 6 hertz. L’index de la main entre en contact avec le pouce et exécute un mouvement circulaire connu sous le nom de roulement de pilule qui est la caractéristique stratégique du tremblement de repos.
La lenteur des mouvements, également connue sous le nom de bradykinésie, est une autre caractéristique cruciale de la maladie de Parkinson. Comme son nom l’indique, ce symptôme connaît des difficultés à effectuer des mouvements. Les mouvements séquentiels et simultanés deviennent intolérables. Ce symptôme devient plus pénétrant dans les phases ultérieures de la maladie. Les symptômes immédiats de la bradykinésie sont des difficultés à effectuer des activités quotidiennes comme écrire, s’habiller, etc., car le contrôle de la motricité fine est requis.
 Le prochain symptôme distinctif de la maladie de Parkinson est la rigidité qui peut être reconnue par l’incapacité du membre à effectuer un mouvement. La rigidité est causée par une augmentation du tonus musculaire due à une contraction disproportionnée et incessante des muscles. La rigidité peut être uniforme ou irrégulière dans le parkinsonisme. Le terme rigidité à crémaillère peut être appliqué lorsque des tremblements et une augmentation du tonus musculaire entrent en jeu. La rigidité peut être associée à des douleurs articulaires car il s’agit du symptôme le plus précoce de la maladie de Parkinson. La rigidité peut être disproportionnée car elle a tendance à perturber les muscles du cou et des épaules en premier.
Le prochain symptôme distinctif de la maladie de Parkinson est la rigidité qui peut être reconnue par l’incapacité du membre à effectuer un mouvement. La rigidité est causée par une augmentation du tonus musculaire due à une contraction disproportionnée et incessante des muscles. La rigidité peut être uniforme ou irrégulière dans le parkinsonisme. Le terme rigidité à crémaillère peut être appliqué lorsque des tremblements et une augmentation du tonus musculaire entrent en jeu. La rigidité peut être associée à des douleurs articulaires car il s’agit du symptôme le plus précoce de la maladie de Parkinson. La rigidité peut être disproportionnée car elle a tendance à perturber les muscles du cou et des épaules en premier.
Au fur et à mesure que la maladie progresse, la rigidité affecte tous les mouvements du corps. L’instabilité posturale survient dans la phase ultérieure de la maladie, provoquant une altération de l’équilibre et les os risquent de se fracturer sans effort. Ce symptôme est généralement inattentif chez les jeunes patients car il monte dans la phase ultérieure de la maladie. Environ 40 % des patients chutent très fréquemment et environ 10 % des patients font une chute hebdomadaire, ce qui montre la gravité de la maladie.
D’autres problèmes moteurs englobent les troubles de la démarche et de la posture tels que les troubles de la festination, de la parole et de la déglutition tels que les troubles de la voix. La rigidité peut être disproportionnée car elle a tendance à perturber les muscles du cou et des épaules en premier.
Les problèmes neuropsychiatriques font également partie intégrante de la maladie de Parkinson et peuvent aller de légers à graves. Ces problèmes comprennent des troubles de la cognition, de l’humeur, du comportement et des processus de pensée. Des problèmes cognitifs peuvent survenir aux stades préliminaires de la maladie et peuvent augmenter à mesure que la maladie progresse. La perturbation cognitive la plus fréquente est le dysfonctionnement exécutif qui peut être caractérisé par des problèmes liés à la pensée abstraite, à la flexibilité cognitive, à des actions inappropriées et à la sélection d’informations sensorielles pertinentes. La vitesse cognitive lente et les fluctuations de l’attention sont d’autres problèmes. Les problèmes visuo-spatiaux ne sont pas non plus rares. Une personne souffrant de la MP a deux à six fois plus de risques d’être atteinte de démence par rapport à la population normale.
Les altérations de l’humeur et du comportement sont très fréquentes chez les patients atteints de maladie de Parkinson avec démence. Ces altérations sont également présentes chez les patients sans troubles cognitifs. La dépression, l’anxiété et l’apathie sont les altérations de l’humeur les plus courantes. L’abus de médicaments et l’envie impérieuse, l’hypersexualité est également courante et est liée au médicament utilisé dans la gestion de la maladie. Des délires et des hallucinations ont été signalés chez environ 4 % des patients. Ce symptôme est le résultat de l’excès dopaminergique.
La maladie de Parkinson peut également perturber d’autres fonctions du corps. Les troubles du sommeil sont très fréquents en cas de maladie de Parkinson et peuvent être aggravés par les médicaments. Les troubles du sommeil comprennent la somnolence et l’insomnie. Les altérations du système nerveux autonome provoquent une peau grasse, une hypotension orthostatique, une transpiration excessive, une fonction sexuelle altérée et une miction incontrôlée. Les problèmes gastriques et la constipation deviennent également graves et peuvent compromettre la santé du patient. Les problèmes liés aux yeux et à la vision entrent également en action et comprennent une diminution du taux de clignement, des yeux secs, des mouvements saccadés, une diminution de la poursuite oculaire et une vision floue. Une altération de l’odorat et une sensation de douleur suivie de paresthésie sont également observées. Ces symptômes font leur apparition bien avant le diagnostic de la maladie.
Causes
La plupart des patients atteints de la maladie de Parkinson peuvent être classés dans la catégorie des maladies idiopathiques car la cause méticuleuse de la maladie est inconnue. Une partie très insignifiante des cas peut être cogitée sous la catégorie des facteurs génétiques.
D’autres facteurs peuvent être classés dans la catégorie des éléments à risque pouvant causer la maladie de Parkinson mais la relation précise entre eux et la maladie est encore vague. La maladie de Parkinson est généralement considérée comme une maladie non génétique, mais dans environ 5 % des cas, une mutation dans certains gènes non ambigus peut entraîner cette maladie.
 Les gènes, à savoir SNCA, UCH-L1, PRKN, LRRK2, PINK1, DJ-1 et ATP13A2 codent pour l’alpha-synucléine, l’ubiquitine carboxy-terminal hydrolase L1, la parkin, la kinase répétée riche en leucine 2, la kinase 1 putative induite par PTEN et les mutations dans l’un de ces gènes peut entraîner la MP. La mutation du gène LRRK2 augmente les chances d’apparition de la MP par rapport à d’autres gènes. SNCA et LRRK2 sont les gènes liés à la MP les plus étudiés. Des mutations dans SNCA, LRRK2 et la glucocérébrocidase (GBA) augmentent le risque de MP sporadique. Des mutations dans la GBA entraînent la maladie de Gaucher.
Les gènes, à savoir SNCA, UCH-L1, PRKN, LRRK2, PINK1, DJ-1 et ATP13A2 codent pour l’alpha-synucléine, l’ubiquitine carboxy-terminal hydrolase L1, la parkin, la kinase répétée riche en leucine 2, la kinase 1 putative induite par PTEN et les mutations dans l’un de ces gènes peut entraîner la MP. La mutation du gène LRRK2 augmente les chances d’apparition de la MP par rapport à d’autres gènes. SNCA et LRRK2 sont les gènes liés à la MP les plus étudiés. Des mutations dans SNCA, LRRK2 et la glucocérébrocidase (GBA) augmentent le risque de MP sporadique. Des mutations dans la GBA entraînent la maladie de Gaucher.
Le rôle de la SNCA est très vital dans la MP car ce gène est responsable de la formation d’une protéine connue sous le nom d’alpha-synucléine qui est l’élément principal des corps de Lewy. Des mutations faux-sens du gène suivies d’une duplication et d’une triplication du locus ont été observées dans des groupes atteints de MP familiale. Bien que les mutations faux-sens soient intermittentes, la multiplication du locus SNCA représente 2% des cas de MP familiale. Des multiplications ont été observées chez les porteurs asymptomatiques. Le gène LRRK2 code pour une protéine appelée dardarine. Les mutations du gène LRRK2 sont principalement responsables de la MP sporadique et familiale. Elle représente 10 % des cas familiaux et 3 % des cas sporadiques de MP. Selon une estimation, environ 40 mutations différentes dans les gènes se sont avérées responsables de la MP.
Pathologie
Un groupe de structures cérébrales innervées par le système dopaminergique et identifiées comme des noyaux gris centraux sont gravement endommagés dans la maladie de Parkinson. Les cellules des régions de la substantia nigra et de la pars compact meurent très fréquemment. Des altérations macroscopiques peuvent être identifiées dans les surfaces coupées du tronc cérébral en raison d’une perte neuronale. La pigmentation mélanique diminue également dans la substantia nigra et le locus coeruleus. L’histopathologie de la substance noire et d’autres régions du cerveau montre une perte neuronale importante ainsi qu’une accumulation importante de corps de Lewy. La perte neuronale est suivie de la mort des astrocytes et de l’activation de la microglie. La présence de corps de Lewy dans différentes régions du cerveau est la caractéristique clé de ce trouble.
Les noyaux gris centraux sont connectés à d’autres zones du cerveau par cinq voies principales. Ces voies sont des circuits moteurs, oculomoteurs, associatifs, limbiques et orbitofrontaux. Dans la maladie de Parkinson, tous ces circuits sont perturbés et le patient souffre de problèmes liés au mouvement, à l’attention et à l’apprentissage. Sur l’ensemble des cinq circuits, le circuit moteur a été intensivement étudié. Un modèle conceptuel est en pratique depuis 1980 qui montre une relation directe entre l’altération du circuit moteur et l’apparition des symptômes de la maladie de Parkinson. Le modèle est cependant modifié avec les avancées récentes de la recherche mais est toujours utilisé encore aujourd’hui.
Selon ce modèle, les noyaux gris centraux exercent une influence inhibitrice sur un large éventail de systèmes moteurs qui les empêche d’être actifs à des moments inappropriés. Lorsqu’une action motrice particulière doit être effectuée, cet effet inhibiteur est réduit. Cet effet inhibiteur diminue avec la libération de dopamine. Des niveaux élevés de dopamine sont nécessaires pour effectuer des actions motrices, mais si le niveau de dopamine diminue, les symptômes de la maladie de Parkinson ont la possibilité de faire leur apparition. La condition dans laquelle le niveau de dopamine diminue est connue sous le nom d’hypokinésie et provoque des difficultés dans les actions motrices.
Les médicaments utilisés pour traiter la maladie de Parkinson peuvent produire des niveaux élevés et excessifs de dopamine entraînant l’activation des systèmes moteurs à des moments inappropriés provoquant des dyskinésies. La condition dans laquelle le niveau de dopamine diminue est connue sous le nom d’hypokinésie et provoque des difficultés dans les actions motrices. Les médicaments utilisés pour traiter la maladie de Parkinson peuvent produire des niveaux élevés et excessifs de dopamine entraînant l’activation des systèmes moteurs à des moments inappropriés provoquant des dyskinésies. La condition dans laquelle le niveau de dopamine diminue est connue sous le nom d’hypokinésie et provoque des difficultés dans les actions motrices. Les médicaments utilisés pour traiter la MP peuvent produire des niveaux élevés et excessifs de dopamine entraînant l’activation des systèmes moteurs à des moments inappropriés provoquant des dyskinésies.
Un certain nombre de mécanismes sont connus dans lesquels la perte de cellules cérébrales est observée. L’un de ces mécanismes consiste en l’accumulation anormale d’une protéine connue sous le nom d’alpha-synucléine. Cette protéine se combine avec l’ubiquitine et entraîne une perte neuronale. Cette protéine s’accumule à l’intérieur des cellules sous forme d’inclusions appelées corps de Lewy. Selon la mise en scène de Braak, les corps de Lewy font d’abord leur apparition dans le bulbe olfactif, la moelle allongée et le tegmentum pontique.
Au fur et à mesure que la maladie progresse, les corps de Lewy commencent à s’accumuler dans la substance noire, les zones du mésencéphale et du cerveau antérieur basal et plus tard dans le néocortex. Ces zones sont les principaux sites où se produit une perte neuronale importante. Les corps de Lewy peuvent ne pas être responsables de la mort cellulaire et peuvent être protecteurs. Chez les patients souffrant de démence, une forte accumulation de corps de Lewy a été observée dans les régions corticales. Des enchevêtrements neurofibrillaires et des plaques séniles peuvent être observés chez les patients atteints de la maladie d’Alzheimer avec démence.
D’autres mécanismes associés à la mort cellulaire sont le dysfonctionnement protéosomique et lysosomal suivi d’une activité mitochondriale réduite. Une accumulation de fer a été remarquée dans les régions de la substance noire.
Diagnostic
La maladie de Parkinson peut être diagnostiquée par des antécédents médicaux et un examen neurologique. Il n’existe à l’heure actuelle aucun test de laboratoire précis disponible qui puisse indiquer clairement qu’une personne souffre de la maladie de Parkinson, bien que les scintigraphies cérébrales aident à identifier la maladie, mais les chances de précision sont faibles. Les patients peuvent recevoir de la lévodopa, ce qui entraîne une réduction des problèmes de déficience motrice et la maladie peut être diagnostiquée avec une plus grande précision. L’isolement des corps de Lewy du mésencéphale par autopsie confirme également qu’une personne souffre de la maladie de Parkinson.
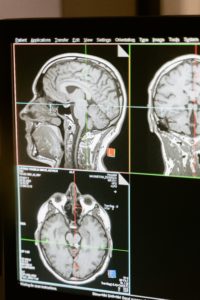 La maladie d’Alzheimer, les infarctus cérébraux multiples et le parkinsonisme d’origine médicamenteuse peuvent également produire le syndrome parkinsonien. Les organisations médicales ont créé certains critères selon lesquels la maladie peut être diagnostiquée à un stade précoce. Les critères les plus largement utilisés ont été développés par le UK Parkinson’ s Banque de cerveaux de la Société des maladies et Institut national américain des troubles neurologiques et des accidents vasculaires cérébraux. La banque de cerveaux de la PD Society se concentre sur les tremblements de repos, la lenteur des mouvements et l’instabilité posturale.
La maladie d’Alzheimer, les infarctus cérébraux multiples et le parkinsonisme d’origine médicamenteuse peuvent également produire le syndrome parkinsonien. Les organisations médicales ont créé certains critères selon lesquels la maladie peut être diagnostiquée à un stade précoce. Les critères les plus largement utilisés ont été développés par le UK Parkinson’ s Banque de cerveaux de la Société des maladies et Institut national américain des troubles neurologiques et des accidents vasculaires cérébraux. La banque de cerveaux de la PD Society se concentre sur les tremblements de repos, la lenteur des mouvements et l’instabilité posturale.
La tomodensitométrie (CT) et l’imagerie par résonance magnétique (IRM) du cerveau des patients atteints de maladie de Parkinson semblent normales. Ces techniques peuvent être utiles dans l’identification des symptômes secondaires de la maladie de Parkinson comme les tumeurs des noyaux gris centraux, la pathologie vasculaire et l’hydrocéphalie. L’IRM de diffusion est cependant utile dans la différenciation du parkinsonisme typique et atypique, mais des recherches supplémentaires sont nécessaires dans ce domaine. Les radiotraceurs TEP et SPECT peuvent être utilisés pour mesurer l’activité des neurones dopaminergiques dans les noyaux gris centraux. Une activité dopaminergique réduite dans les neurones des noyaux gris centraux peut être un indice de ce trouble.
La gestion
Dans le scénario actuel, il n’y a pas de remède possible pour la maladie de Parkinson, mais les médicaments, la chirurgie et la gestion multidisciplinaire peuvent aider les patients à survivre. Les médicaments les plus prometteurs utilisés pour guérir les symptômes moteurs sont la lévodopa, les agonistes de la dopamine et les inhibiteurs de la MAO-B. Ces médicaments sont généralement prescrits en fonction de la phase de la maladie associée.
En termes généraux, deux étapes des médicaments sont identifiées. Dans la phase initiale, le patient atteint de la maladie de Parkinson développe un certain handicap pour lequel il a besoin d’un traitement pharmacologique et dans la seconde phase, le patient développe des symptômes moteurs liés à l’utilisation de la lévodopa. Le traitement au stade initial vise à minimiser les effets secondaires résultant de l’augmentation de l’activité dopaminergique.
Le début du traitement par la lévodopa peut être retardé par l’utilisation d’autres médicaments comme les agonistes de la dopamine et les inhibiteurs de la MAO-B. Ces médicaments peuvent retarder l’apparition des dyskinésies. La deuxième phase de la médication vise à réduire les fluctuations qui ont résulté du traitement. Lorsque les médicaments ne donnent pas les résultats souhaités, des méthodes de chirurgie et de stimulation cérébrale profonde sont utilisées. Aux derniers stades de la maladie, des soins palliatifs sont dispensés afin d’améliorer la qualité de vie.
Lévodopa
La lévodopa est utilisée pour le traitement de la maladie de Parkinson depuis plus de 30 ans. Dans les neurones dopaminergiques, la L-DOPA est convertie en dopamine en présence de dopa décarboxylase. Comme les symptômes moteurs de la MP sont causés par le manque de dopamine dans les cellules de la substance noire, l’administration de L-DOPA peut aider à diminuer temporairement les symptômes moteurs.
Des études ont indiqué que seulement 5 à 10 % de la L-DOPA traverse la barrière hémato-encéphalique. Bien que la L-DOPA soit convertie en dopamine, elle produit également un certain nombre d’effets secondaires tels que des nausées, des dyskinésies et des raideurs articulaires. La carbidopa et le bensérazide sont de puissants inhibiteurs périphériques de la dopa décarboxylase. Ils bloquent la conversion de la L-DOPA en dopamine et réduisent donc les effets secondaires en augmentant la biodisponibilité. La lévodopa est également liée au syndrome de dérégulation de la dopamine qui est le résultat d’une surutilisation du médicament. Si les doses de lévodopa sont administrées par voie intraveineuse et par perfusions intestinales, la vitesse de propagation du médicament augmente.
Le tolcapone est connu pour inhiber l’activité de l’enzyme COMT qui est responsable de la dégradation de la dopamine et cela prolonge à son tour l’activité de la lévodopa. L’utilisation de lévodopa dans les phases ultérieures de la maladie entraîne des mouvements involontaires également connus sous le nom de dyskinésies et des fluctuations en réponse aux médicaments. Lorsque cela se produit, le patient atteint de la MP passe d’une bonne réponse aux médicaments et peu de symptômes à aucune réponse aux médicaments et à des symptômes moteurs importants. Par conséquent, il est conseillé de maintenir les doses de lévodopa faibles afin de maintenir la stabilité fonctionnelle du patient. L’utilisation d’alternatives à la lévodopa est désormais pratique.
Agonistes dopaminergiques
On connaît un certain nombre d’agonistes de la dopamine qui ont des effets similaires à ceux de la lévodopa et sont connus pour se lier aux récepteurs post-synaptiques dopaminergiques. Ils sont généralement utilisés pour les personnes souffrant de dyskinésies et les exemples courants sont la bromocriptine, le pergolide, le piribédil, l’apomorphine et le lisuride.
Bien qu’ils soient connus pour produire des effets importants, ils provoquent également des effets secondaires bénins, à savoir la somnolence, les hallucinations, l’insomnie, les nausées et la constipation. Parfois, à des doses très légères, des effets secondaires apparaissent et le médecin doit donc rechercher un autre médicament.
Ces médicaments sont utiles pour guérir les symptômes moteurs causés par l’abus de médicaments et sont utiles pour traiter les symptômes qui surviennent pendant les phases initiales de la maladie. Ils sont plus chers que la lévodopa et les dyskinésies dues aux agonistes dopaminergiques sont cependant,
Inhibiteurs de la MAO-B
Ces médicaments sont connus pour augmenter les niveaux de dopamine dans les noyaux gris centraux en bloquant leur métabolisme. Ils sont connus pour inhiber l’activité de la monoamine oxydase-B qui décompose la dopamine sécrétée par les neurones dopaminergiques. La réduction de l’activité de la MAO-B augmente les niveaux de L-DOPA dans le striatum. Ils sont utilisés pour améliorer les symptômes moteurs dans les phases précoces de la maladie mais sont moins efficaces que la lévodopa. Ils produisent plus d’effets secondaires.
Chirurgie et stimulation cérébrale profonde
Les chercheurs pensaient plus tôt que la chirurgie et la stimulation cérébrale profonde peuvent aider à traiter les symptômes moteurs de la MP, mais avec la découverte de la lévodopa, le nombre d’opérations a fortement chuté. La chirurgie est généralement effectuée dans les cas où les médicaments ne produisent pas d’effet significatif. La chirurgie en cas de maladie de Parkinson peut être classée dans deux groupes, à savoir la stimulation cérébrale lésionnelle et profonde (DBS). Les zones cibles des lésions et de la DBS sont le thalamus et le noyau sous-thalamique. Le DBS est le traitement chirurgical le plus couramment utilisé et il implique l’utilisation d’un stimulateur cérébral qui envoie des impulsions électriques à des zones spécifiques du cerveau. Le DBS est généralement utilisé pour les personnes qui souffrent de fluctuations motrices et de tremblements incontrôlés ou pour celles qui souffrent de graves problèmes neuropsychiatriques.
Rééducation et régime
 Les problèmes d’élocution peuvent être guéris grâce à la rééducation, bien que des recherches supplémentaires soient nécessaires dans ce domaine. L’exercice physique régulier avec ou sans physiothérapie peut être utile pour traiter les problèmes liés à la mobilité, la flexibilité, la démarche, etc. bien que le programme d’exercices doive être pratiqué sous la stricte supervision du physiothérapeute. Les muscles et les nerfs qui contrôlent le processus digestif sont généralement affectés dans la maladie de Parkinson, entraînant constipation et gastroparésie. Une alimentation équilibrée est recommandée par les médecins car des difficultés de déglutition peuvent survenir à mesure que la maladie progresse.
Les problèmes d’élocution peuvent être guéris grâce à la rééducation, bien que des recherches supplémentaires soient nécessaires dans ce domaine. L’exercice physique régulier avec ou sans physiothérapie peut être utile pour traiter les problèmes liés à la mobilité, la flexibilité, la démarche, etc. bien que le programme d’exercices doive être pratiqué sous la stricte supervision du physiothérapeute. Les muscles et les nerfs qui contrôlent le processus digestif sont généralement affectés dans la maladie de Parkinson, entraînant constipation et gastroparésie. Une alimentation équilibrée est recommandée par les médecins car des difficultés de déglutition peuvent survenir à mesure que la maladie progresse.
Dans certains cas, la gastrotomie est pratiquée lorsque la nourriture est délivrée directement dans l’estomac. Une forte concurrence se produit entre les protéines et la lévodopa, car les deux utilisent le même système de transport dans l’intestin et la barrière hémato-encéphalique. Lorsque les deux sont pris ensemble, l’efficacité du médicament diminue. Par conséquent, lorsque la lévodopa est prise, les régimes riches en protéines sont abandonnés et il est suggéré au patient de suivre un régime méditerranéen équilibré.
Soins palliatifs et axes de recherche
Les soins palliatifs sont généralement requis dans les phases finales de la maladie lorsque toutes les stratégies médicamenteuses deviennent inefficaces. L’objectif premier des soins palliatifs est d’améliorer la qualité de vie du patient. Un soutien familial fort est très efficace à cet égard. La maladie de Parkinson est la deuxième maladie neurodégénérative la plus dangereuse après la maladie d’Alzheimer. Nous pouvons finir par dire que la DP doit être prise au sérieux car elle a le potentiel d’empirer la vie d’un individu si elle est négligée.
Par Navodita Maurice
Cet article pourrait intéresser un de vos amis ami ou un de vos proches ? N’hésitez pas à le partager. Le Partage c’est La Vie !!!

Télécharger le guide
"Pour Réussir"
Dans ce petit guide gratuit vous découvrirez
18 Secrets de Grand Leaders
pour développer votre confiance en soi.

